Artículos de Investigación
¿Audífono o implante coclear? Una propuesta razonada para decidir cuál es el momento de indicar un implante coclear
Enrique A. Lopez-Poveda1, 2, 3 , Miriam I. Marrufo-Pérez1, 2, 3
, Miriam I. Marrufo-Pérez1, 2, 3
1 Instituto de Neurociencias de Castilla y León (INCYL), Universidad de Salamanca, España / 2 Instituto de Investigación Biomédica de Salamanca (IBSAL), Universidad de Salamanca, España / 3 Departamento de Cirugía, Facultad de Medicina, Universidad de Salamanca, España
 OPEN ACCESS
OPEN ACCESS
PEER REVIEWED
ARTÍCULO ORIGINAL
DOI: 10.51445/sja.auditio.vol9.2025.120
Recibido: 25.06.2025
Revisado: 03.07.2025
Aceptado: 06.08.2025
Publicado: 29.10.2025
Editado por:
Óscar M. Cañete
School of Psychology, University of Auckland, New Zealand.
Revisado por:
Virginia Olivares
Escuela de Fonoaudiologia, Universidad de Valparaiso, Chile.
Ángel Ramos de Miguel
Universidad de Las Palmas de Gran Canaria, España.
Verónica Del Vecchio
Asociación Argentina de Audiologia (ASARA), Argentina.
Cómo citar:
Lopez-Poveda, E. A. y Marrufo-Pérez, M. I. (2025). ¿Audífono o implante coclear? Una propuesta razonada para decidir cuál es el momento de indicar un implante coclear. Auditio, 9, e120. https://doi.org/10.51445/sja.auditio.vol9.2025.120
Correspondencia:
Enrique A. Lopez-Poveda
Instituto de Neurociencias de Castilla y León, Universidad de Salamanca, Calle Pintor Fernando Gallego 1, 37007 Salamanca, España. Email: ealopezpoveda@usal.es
 CC-BY 4.0
CC-BY 4.0
© 2025 Los autores / The authors
https://journal.auditio.com/
Publicación de la Asociacion Española de Audiología (AEDA)
Resumen
El implante coclear (IC) fue aprobado como tratamiento de la hipoacusia profunda en 1985 en Estados Unidos y en 1995 en España. Desde entonces, los criterios de indicación del IC han evolucionado en paralelo con los avances científicos y tecnológicos de dichos dispositivos. Actualmente, las personas con hipoacusia severa (≥70 dB HL) bilateral son candidatas a IC en la mayoría de los países. El objetivo de este estudio es investigar si pacientes ‘límite’, es decir, que no llegan a sufrir una hipoacusia severa, podrían rendir mejor con ICs que con audífonos. La evidencia científica analizada demuestra que los pacientes con umbrales audiométricos medios (0.5-2 kHz) de 65 dB HL tienen un 80 % de probabilidad de rendir mejor con un IC que con uno o dos audífonos. La evidencia también demuestra que el reconocimiento de palabras monosilábicas es más sensible para detectar candidatos a IC que el reconocimiento de frases. Las personas con un reconocimiento de palabras preoperatorio menor al 60 % en la mejor condición de escucha van a mostrar mayor rendimiento con IC y audífono contralateral que con dos audífonos. La implantación reduce el impacto emocional y social de la pérdida auditiva y aumenta la calidad de vida de esas personas. Nuestra síntesis concuerda con estudios recientes e informes internacionales que sugieren que los profesionales deberían considerar remitir a los pacientes para evaluar su candidatura a IC cuando tengan umbrales audiométricos >60-65 dB HL y reconocimiento de palabras <60 % en la mejor condición de escucha.
Palabras clave
Hipoacusia, reconocimiento de habla, satisfacción, calidad de vida.
Implicaciones clínicas
Tratar la pérdida auditiva de forma óptima es primordial para paliar su impacto negativo tanto en los pacientes como en la sociedad. Existe una amplia gama de dispositivos para tratar la pérdida auditiva, entre los que se incluyen audífonos e implantes cocleares (ICs). En este artículo analizamos los criterios actuales de indicación de los ICs en España y en otros países. Motivados por el hecho de que esos criterios van evolucionando en paralelo con los avances científicos y tecnológicos, revisamos la literatura especializada para saber si los usuarios de audífonos que no alcanzan hipoacusia severa podrían rendir mejor con ICs. La evidencia científica muestra que los pacientes con hipoacusia moderada (umbrales >60-65 dB HL) y reconocimiento de palabras <60 % en la mejor condición de escucha tienen más probabilidad de rendir mejor con ICs que con audífonos.
Introducción
La pérdida de audición es la tercera discapacidad más común en el mundo (British Deaf Association, 2015). Más de 1.500 millones de personas (el 19 % de la población mundial) sufren algún grado de pérdida auditiva y 430 millones requieren tratamiento (OMS, 2025). La pérdida de audición no tratada incrementa en un 8 % el riesgo de desarrollar demencia (Livingston et al., 2024) y está asociada a sentimientos de soledad y aislamiento social (Shukla et al., 2020), dos fenómenos que aumentan la mortalidad y la probabilidad de sufrir enfermedades cardiovasculares (Leigh-Hunt et al., 2017; Livingston et al., 2024). Como consecuencia, cada año se pierde un billón de dólares en el mundo debido a un inadecuado o nulo abordaje de la pérdida de audición (OMS, 2021). Es primordial tratar la pérdida auditiva de forma óptima para reducir su enorme impacto negativo tanto en el paciente como en la sociedad.
Existe una amplia gama de dispositivos para tratar la pérdida auditiva, entre los que se incluyen audífonos e implantes cocleares (ICs). En este artículo analizamos los criterios actuales para la indicación de estos dispositivos en España y en otros países. Dado que los criterios varían de unos países a otros, y que esos criterios van evolucionando en paralelo con los avances científicos y tecnológicos, hemos revisado la literatura especializada para dar respuesta a la siguiente pregunta: ¿podrían algunos usuarios de audífonos que no cumplen los actuales criterios de implantación rendir mejor con ICs?
Indicaciones y limitaciones de los audífonos
Los audífonos amplifican los sonidos para compensar la pérdida de sensibilidad auditiva y son la opción de tratamiento más común para las personas con pérdida auditiva neurosensorial moderada (40-70 dB HL). A pesar de que estos dispositivos restauran la audibilidad de los sonidos, las personas que los utilizan suelen mostrar más dificultades para entender el habla que las personas normoyentes (Alkaf y Firszt, 2007; Leigh et al., 2016; Lopez-Poveda et al., 2017; Peters et al., 1998). Esto puede observarse en la Figura 1A, donde se muestra que el rendimiento de los usuarios de audífonos en tareas de reconocimiento del habla es peor cuanto mayor es la pérdida auditiva. Esta dificultad se debe tanto a limitaciones de los propios audífonos como a la peor codificación del habla en el sistema auditivo dañado.
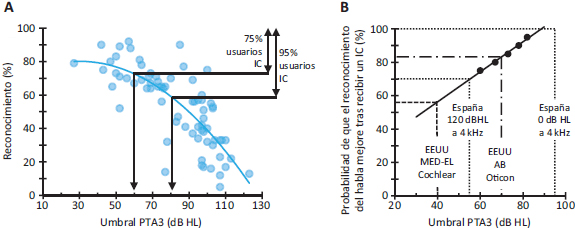
Figura 1. A. Reconocimiento de fonemas en silencio en usuarios de audífonos en función del umbral audiométrico medio a 0.5, 1 y 2 kHz (umbral PTA3) (N=76). El reconocimiento se midió con uno o dos audífonos. El umbral PTA3 se midió sin amplificación. Las líneas horizontales indican que el 75 % y el 95 % de los usuarios de IC mostraban un reconocimiento de fonemas ≥73 y 58 %, respectivamente. Estos valores de reconocimiento corresponden a los obtenidos por usuarios de audífonos con umbrales PTA3 de 60 y 82 dB HL, respectivamente, de acuerdo con el ajuste realizado a los datos (véanse las dos flechas más a la izquierda). Figura adaptada de Leigh et al. (2016). B. Probabilidad de que el reconocimiento del habla en los usuarios de audífonos mejore cuando reciben un IC en función del umbral PTA3 (medido sin amplificación). Los puntos corresponden a los datos inferidos por Leigh et al. (2016) y la línea continua ilustra un ajuste lineal a los datos. Las líneas de puntos y rayas muestran los umbrales audiométricos que debe tener una persona adulta con pérdida auditiva bilateral para ser candidata a IC en diferentes países y para diferentes marcas (Tabla 1). AB: Advanced Bionics.
Por un lado, a medida que la pérdida auditiva aumenta, se reduce el rango de niveles sonoros que el oyente puede percibir. Por tanto, el audífono debe amplificar y, a la vez, comprimir considerablemente los niveles sonoros del habla para que esta sea audible sin llegar a resultar molesta. Si el rango de niveles sonoros se comprime en exceso, es más probable que el habla se distorsione, especialmente cuando el audífono es de acción rápida, lo que dificulta la comprensión del habla (e. g., Jorgensen et al., 2018). Además, el habla también puede distorsionarse porque determinados segmentos alcanzan el nivel máximo de salida que puede aportar el audífono (Davies-Venn et al., 2009).
Por otro lado, a mayor pérdida auditiva, más probable es que haya una disfunción o una pérdida de células ciliadas internas y/o de sinapsis cocleares, dando lugar a regiones cocleares muertas y, por tanto, a que parte de la información del habla no sea transmitida por esas regiones (Johannesen et al., 2014; Jorgensen et al., 2018). Esto genera déficits en el procesamiento temporal y espectral de la información del habla, haciendo que los usuarios de audífonos reconozcan el habla peor de lo esperado según su audibilidad. En otras palabras, la persona oye el habla, pero tiene dificultades para entenderla (Jorgensen et al., 2018; Souza et al., 2007; Summers et al., 2013).
Otra limitación del audífono es que, al amplificar las frecuencias sonoras que de otro modo resultarían inaudibles para el paciente, puede hacer que esas frecuencias se perciban a través de regiones tonotópicas cocleares que no corresponden a dichas frecuencias. Es decir, puede ocurrir que las frecuencias del sonido más amplificadas se perciban fuera de su región tonotópica natural, dificultando así la detección y discriminación de otras frecuencias del sonido menos amplificadas. Esta limitación también puede dar lugar a que el usuario del audífono oiga el habla, pero no pueda reconocerla, sobre todo cuando el habla se presenta junto con otros sonidos o en ambientes ruidosos (Lopez-Poveda et al., 2017).
El IC también tiene limitaciones (Carlyon y Goehring, 2021). Por ejemplo, al igual que el audífono, el IC debe comprimir el rango de niveles sonoros del habla a un rango mucho más estrecho de niveles de carga eléctrica (Lopez-Poveda et al., 2016, 2017, 2020). Además, el IC codifica los sonidos con una resolución espectral pobre, debido tanto al limitado número de canales de su procesador de audio como al número de electrodos que puede activar simultáneamente (Zhang et al., 2025). Sin embargo, el IC estimula el nervio auditivo directamente y, por tanto, puede conducir el sonido a través de fibras del nervio auditivo que inervan regiones cocleares muertas. Por otro lado, aunque la estimulación eléctrica también puede dispersarse a fibras del nervio auditivo tonotópicamente distantes, dicha limitación puede controlarse parcialmente mediante estrategias de codificación o la programación del IC.
Por todo ello, cabe preguntarse: ¿es posible que el IC resulte ventajoso cuando el audífono ya no lo es? Más concretamente: ¿a partir de qué grado de pérdida auditiva rendiría una persona mejor con un IC que con uno o dos audífonos?
Criterios de indicación del implante coclear
Son varios y diversos los requisitos que debe cumplir una persona para ser candidata a IC. Algunos de ellos son inherentes a la funcionalidad del dispositivo y, por tanto, comunes en todos los países. Por ejemplo, se requiere que la persona tenga una cóclea desarrollada, así como un nervio auditivo y una vía auditiva central funcionales. Otros criterios, sin embargo, tienen que ver con el grado de pérdida auditiva de la persona y con el rendimiento que alcanza en tareas de reconocimiento de habla con su(s) audífono(s). Al contrario que los primeros, estos otros criterios varían de un país a otro.
En 1985, la Food and Drug Administration (FDA) de Estados Unidos aprobó el uso de ICs en adultos con pérdida auditiva profunda (>90 dB HL) bilateral postlocutiva. En España, el IC fue aprobado como tratamiento de la hipoacusia profunda por la Agencia de Evaluación de Tecnologías Sanitarias (Instituto de Salud Carlos III) en 1995. Desde entonces, los criterios de indicación han evolucionado de tal forma que cada vez un mayor número de personas se consideran candidatas a IC (revisado por Park et al., 2021; Zwolan y Basura, 2021). No obstante, no hay unanimidad entre países con respecto a estos criterios.
Los criterios actuales de implantación en Reino Unido, España, y Estados Unidos se resumen en la Tabla 1. Si nos centramos, por ejemplo, en adultos con pérdida auditiva bilateral, podemos ver que en Reino Unido son candidatos a IC si tienen umbrales ≥80 dB HL en dos o más frecuencias entre 0.5 y 4 kHz (NICE, 2019). En España, deben tener umbrales >70 dB HL “en el rango de frecuencias conversacionales (desde 0.5 a 4 kHz)” (Manrique et al., 2017), sin especificar si la pérdida auditiva debe darse en todas y cada una de las frecuencias o si se refiere al promedio de los umbrales de todas ellas. En Estados Unidos existen diferencias en las indicaciones de la FDA para las diferentes marcas de ICs. Por ejemplo, un adulto con pérdida auditiva bilateral es candidato a recibir un IC de la compañía MED-ELTM si tiene un umbral medio >40 dB HL para bajas frecuencias (0.25, 0.5 y 1 kHz) y >65 dB HL para altas frecuencias (3-8 kHz) (FDA, 2024). Sin embargo, el umbral medio a 0.5, 1 y 2 kHz (denominado PTA3) debe ser ≥70 dB HL para recibir el dispositivo de Oticon (Zwolan y Basura, 2021). Desconocemos el motivo por el cual las frecuencias audiométricas utilizadas para estimar la pérdida auditiva varían entre países.
Tabla 1. Criterios de indicación del IC en Reino Unido, España y Estados Unidos. Los criterios para pérdida unilateral aplican también para pérdida asimétrica.
País |
Dispositivo |
Edad (años) |
Pérdida auditiva |
Grado de pérdida auditiva |
Reconocimiento de habla con audífonos |
Reino Unido (NICE, 2019) |
Todas las marcas de IC, a excepción de Neurelec (no se disponía de datos suficientes) |
≥18 |
Unilateral o bilateral |
≥80 dB HL en 2 o más frecuencias (0.5, 1, 2, 3 y 4 kHz) |
Reconocimiento de fonemas <50 % en la prueba de palabras de Arthur Boothroyd presentada a 70 dB A |
<18 |
Habilidades de habla, lenguaje y comprensión oral no adecuadas a la edad, la etapa de desarrollo y la capacidad cognitiva |
||||
España (Manrique et al., 2017) |
Todas las marcas |
≥18 |
Bilateral |
>70 dB HL (0.5 a 4 kHz) |
<40 % en prueba vocal a 65 dB SPL |
Unilateral |
>70 dB HL oído IC |
<50 % en reconocimiento de bisílabos en silencio a 65 dB SPL |
|||
>6 meses y <18 años |
Bilateral |
>70 dB HL (0.5 a 4 kHz) |
Mínimo beneficio con audífono. Desarrollo del lenguaje y habilidades de escucha no correlacionadas con edad y cognición |
||
<12 |
Unilateral |
>70 dB HL |
|||
Estados Unidos (FDA) |
MED-EL |
≥18 |
Bilateral |
>40 dB HL (media 0.25, 0.5, 1 kHz) y >65 dB HL (media 3-8 kHz) |
≤50 % en el oído que se va a implantar y ≤60 % en el oído no implantado en la prueba de palabras CNC1 grabada |
1-17 |
Bilateral |
≥90 dB HL a 1 kHz |
≤20 % en las pruebas MLNT o LNT2 en mejor condición de escucha |
||
≥5 |
Unilateral |
>90 dB HL |
≤5 % en el oído que se va a implantar en la prueba CNC |
||
Cochlear |
≥18 |
Bilateral |
>40 dB HL en frecuencias bajas y >90 dB HL medias y altas |
<50 % en el oído a implantar y <60 % en la mejor condición de escucha para frases grabadas y en formato abierto |
|
2-17 |
Bilateral |
>70 dB HL |
≤30 % en la prueba MLNT o LNT en mejor condición de escucha |
||
9 meses-2 años |
Bilateral |
>90 dB HL |
Beneficios limitados de la amplificación binaural |
||
≥5 |
Unilateral |
>80 dB HL (media 0.5, 1, 2, 4 kHz) |
≤5 % en la prueba CNC en el oído a implantar |
||
Advanced Bionics |
≥18 |
Bilateral |
>70 dB HL |
≤50 % en el reconocimiento de frases HINT3 en formato abierto |
|
1-17 |
Bilateral |
≥90 dB HL |
≤20 % en la prueba MLNT o LNT |
Notas: 1 Consonant-Nucleus-Consonant test (CNC, Peterson y Lehiste, 1962). 2 Multisyllabic/Lexical Neighborhood Test (MLNT, Kirk et al., 1995). 3 Hearing In Noise Test (HINT, Nilsson et al., 1994).
Con respecto al criterio de rendimiento en tareas de reconocimiento del habla, la Tabla 1 muestra que la prueba utilizada es diferente en los distintos países e incluso para las diferentes marcas dentro de un mismo país. En algunos casos, no se especifica qué tipo de material verbal debe emplearse (frases, palabras o sílabas), el nivel sonoro en el que debe presentarse, si debe presentarse en silencio o con ruido, el tipo de ruido, o a qué relación señal-ruido (SNR) debe evaluarse dicho reconocimiento. A juzgar por la evidencia, sería conveniente establecer un criterio universal respecto al material verbal que debe utilizarse y las condiciones de evaluación.
Objetivos de este trabajo
La variabilidad de los criterios de implantación entre los diferentes países da lugar a que una misma persona pueda ser candidata a IC en un país y no en otro, o que lo sea o no dependiendo de la prueba verbal que se haya utilizado para evaluar su rendimiento con audífonos. Debido a ello, es razonable que tanto a los reguladores como al personal clínico le resulte difícil saber si realmente están ofreciendo el mejor tratamiento a los pacientes. En este sentido, un primer objetivo de este trabajo es determinar qué personas se beneficiarían del uso de ICs frente a audífonos.
Por otro lado, los criterios para recibir ICs han evolucionado a lo largo de los años en paralelo con el avance de la tecnología del IC (Hainarosie et al., 2014). El avance tecnológico de los audífonos está limitado por el propio daño en el sistema auditivo del paciente. Por tanto, un segundo objetivo es revisar si el rendimiento de pacientes ‘límite’ (que no cumplen los criterios de implantación actuales) es mejor con ICs que con audífonos. Nuestra hipótesis es que las personas que no llegan a cumplir los criterios de implantación actuales podrían rendir mejor y estar más satisfechas con un IC y un audífono contralateral que con dos audífonos.
Abordaremos estos objetivos analizando los datos disponibles en la literatura científica. Las variables que se analizarán incluyen “grado de pérdida auditiva”, “rendimiento en pruebas de reconocimiento del habla” y “grado de satisfacción tras recibir un IC”. Puesto que nuestro objetivo es proporcionar una perspectiva sobre un tema relevante para el ámbito clínico, hemos realizado una selección de estudios guiada por su relevancia y actualidad, sin pretender cubrir de forma exhaustiva o sistemática toda la evidencia disponible.
Reconocimiento de habla con implante coclear y con audífono
En esta sección analizaremos diferentes estudios científicos que han comparado el rendimiento de usuarios de IC con el rendimiento de usuarios de audífonos (comparación entre grupos). También analizaremos estudios que han evaluado el rendimiento de personas que no cumplían los criterios de indicación relativos a la pérdida auditiva y/o el rendimiento con audífonos y aun así recibieron un IC (comparación intragrupo).
Comparación entre grupos
Numerosos estudios han evaluado el reconocimiento de habla en silencio y en ruido en usuarios de audífonos. En general, estos estudios han demostrado que el reconocimiento empeora al aumentar la pérdida auditiva, a pesar de que el audífono proporciona la amplificación esperada por la regla de prescripción de ganancia (Lopez-Poveda et al., 2017; Peters et al., 1998; Summers et al., 2013). Ese descenso en el reconocimiento puede verse en la Figura 1A, que muestra el porcentaje de fonemas reconocidos en silencio por 62 personas (con edades entre 4,6 y 16,2 años) en función de su pérdida auditiva (Leigh et al., 2016). La pérdida auditiva se indica como el umbral audiométrico medio a las frecuencias de 0,5, 1 y 2 kHz, en adelante, PTA3. El reconocimiento de fonemas se midió utilizando palabras del tipo consonante-vocal-consonante, o CNC. Los participantes utilizaron audífonos programados con las reglas de prescripción de ganancia NAL-RP o NAL-NL1 (Byrne et al., 2001). El reconocimiento se evaluó de forma bilateral en las personas con pérdida auditiva simétrica (N=48) y en cada oído por separado para las personas con pérdida asimétrica (N=14) (N=76 medidas en total). Las palabras se presentaron a viva voz a 65 dB A o mediante un altavoz (material grabado) a 65 dB SPL. El audiólogo o el altavoz estaban ubicados frente al participante. Puesto que el reconocimiento de fonemas disminuye al aumentar la pérdida auditiva (Figura 1A), cabe esperar que, a partir de una determinada pérdida, las personas muestren mayor rendimiento usando un IC que usando uno o dos audífonos, ya que las personas con IC suelen alcanzar un alto rendimiento en tareas de reconocimiento de habla presentada en silencio (p. ej., ≥90% en Dorman et al., 2000; Amoodi et al., 2012).
Leigh et al. (2016) investigaron a partir de qué grado de pérdida auditiva es más probable que las personas rindan mejor con IC que con audífono(s). Para ello, compararon el rendimiento de usuarios de audífonos (Figura 1A) con el rendimiento de usuarios de IC (N=78, 75 con IC unilateral y 3 bilateral) con edades y características demográficas similares. Los usuarios de IC tenían hipoacusia neurosensorial bilateral prelocutiva (PTA3 ≥ 83 dB HL) antes de la implantación, recibieron el IC multicanal Nucleus® antes de los 3 años, utilizaron el procesador del habla y la estrategia de procesamiento del habla más recientes (ACE o SPEAK) y disponían de 20 o más electrodos activos. Leigh et al. (2016) observaron que el 75 % de los usuarios de IC mostraban un reconocimiento de fonemas ≥73 % cuando percibían el habla a través del oído con IC. Este porcentaje de reconocimiento se correspondía con el que mostraban los usuarios de audífonos con umbrales audiométricos de 60 dB HL (Figura 1A). Esto significa que una persona con umbral PTA3 ≥ 60 dB HL tiene un 75 % de probabilidad de rendir mejor con un IC que con audífonos, al menos cuando el habla se presenta en silencio. Asimismo, el 95 % de los usuarios de IC mostraba un reconocimiento de palabras ≥58 %, que se corresponde con el rendimiento medio de los usuarios de audífonos con umbrales de 82 dB HL (Figura 1A). Por tanto, una persona con umbrales PTA3 ≥ 82 dB HL tiene un 95 % de probabilidad de rendir mejor con un IC que con audífonos.
Para trasladar esas probabilidades a los criterios de indicación actuales, hemos creado la Figura 1B. Esta figura muestra la probabilidad de que las personas con pérdida auditiva bilateral rindan mejor con un solo IC que con uno o dos audífonos. Los cinco puntos corresponden a los dos valores de probabilidad descritos en el párrafo anterior y a tres valores intermedios. La línea representa un ajuste lineal a los cinco puntos, extrapolado a otros umbrales PTA3. Como se indica en la Tabla 1 y en la propia Figura 1B, para que una persona adulta con pérdida auditiva bilateral reciba un implante de MED-EL o Cochlear en Estados Unidos debe tener un umbral promedio para tonos de baja frecuencia >40 dB HL. Según la Figura 1B, una persona con un umbral PTA3 de 40 dB HL tendría un 56 % de probabilidades de rendir mejor con un IC que con audífonos, mientras que una persona con un umbral PTA3 de 70 dB HL tendría un 83 % de probabilidades de rendir mejor con un IC que con audífonos.
Calcular la probabilidad de que un candidato a IC en España rinda mejor con IC que con audífono(s) no es inmediato porque, como se ha dicho antes, los criterios de indicación de IC en España se basan en los umbrales audiométricos a cuatro frecuencias (0.5, 1, 2 y 4 kHz) en lugar de a tres (0.5, 1 y 2 kHz o PTA3) y, a su vez, no se especifica si la pérdida a esas cuatro frecuencias se refiere al promedio o a todas y cada una de ellas. No obstante, se pueden hacer aproximaciones. Suponiendo que el criterio español se refiere a la pérdida media a esas cuatro frecuencias (PTA4) y dado que el criterio para recibir un IC en España es tener un umbral ≥ 71 dB HL (Tabla 1), una persona con un umbral audiométrico de 0 dB HL a 4 kHz recibiría un IC si su umbral PTA3 fuera > 95 dB HL. En cambio, si su umbral a 4 kHz fuese 120 dB HL, recibiría un IC con un PTA3 > 55 dB HL. Según la Figura 1B, estos umbrales PTA3 (55 y 95 dB HL) corresponderían con probabilidades del 70 % y del 100 %, respectivamente, de mostrar mejor rendimiento con un IC que con audífonos. Es decir, en España, una persona es candidata a IC cuando la probabilidad de que rinda mejor con el IC está entre 70 % y 100 %. Por tanto, el criterio español de rendimiento es más restrictivo que el de Estados Unidos.
Es difícil decidir qué probabilidad de mejora debe contemplarse para considerar que una persona sea candidata a IC. Leigh et al. (2016) proponen que se consideren candidatas a personas con PTA3 ≥ 65 dB HL, cuya probabilidad de mejora con el IC sería del 80 %. Sin embargo, en Estados Unidos, para algunas marcas basta una pérdida de PTA3 ≥ 40 dB HL (probabilidad de mejora con IC del 56 %), siempre y cuando haya pérdida auditiva >65 dB HL a frecuencias más altas (Tabla 1). El estudio de Leigh et al. (2016) concuerda con otra investigación más reciente de Zwolan et al. (2020), quienes sugieren que los profesionales deberían considerar remitir a los pacientes para evaluar su candidatura a IC cuando tengan umbrales PTA3 > 60-65 dB HL.
Comparación intragrupo: reconocimiento antes y después de recibir un IC
En esta sección analizaremos los datos de varios estudios para investigar si personas que actualmente no son candidatas a IC muestran mayor reconocimiento de habla en silencio y en ruido tras recibir un implante.
Reconocimiento de habla en silencio
Gifford et al. (2010) evaluaron el reconocimiento de frases (HINT o AzBio) y de palabras (CNC) en 22 adultos con edades de entre 32 y 84 años (media: 64,2 años), e hipoacusia bilateral moderada a profunda (PTA3 ≥ 57 dB HL) que recibieron un IC. El IC pertenecía a una de las dos generaciones más modernas de dispositivos en el momento de la realización del estudio: 15 participantes portaban Cochlear (series N24 o Freedom 24RE), 5 participantes portaban Advanced Bionics (HR90k) y 2 participantes portaban MED-EL (Combi 40 y Sonata). Todos los participantes fueron evaluados cuando llevaban dos audífonos (antes de la implantación) y unilateralmente en el oído con IC tras la implantación. Además, los 18 participantes que usaban audífono en el oído no implantado también fueron evaluados cuando usaban IC y audífono (audición bimodal). Se verificó que la ganancia aportada por los audífonos (en oído real) coincidía con los objetivos de NAL-NL1 a 55, 60 y 70 dB SPL. Todas las evaluaciones se realizaron con sonidos grabados presentados a 60 o 70 dB A a través de un único altavoz situado a 1 m de distancia frente al participante.
Las Figuras 2A y 2E muestran el reconocimiento de frases antes de la implantación en función del PTA3 y PTA4, respectivamente. Cinco participantes no cumplían con los criterios de indicación vigentes en Estados Unidos (Figura 2A). En España, sólo 9 de los 22 participantes habrían sido candidatos a IC si asumimos que el criterio “<40 % en prueba vocal” se refiere al reconocimiento de frases (Figura 2E), y 13 de los 22 habrían sido candidatos si asumimos que el criterio se refiere al reconocimiento de palabras (Figura 2F). Veinte de los 22 participantes mostraron mejor rendimiento con un sólo IC (Figura 2C, G) que en la mejor condición de escucha (i.e., con dos audífonos) antes de recibir el implante (Figura 2B, F). La mejora media fue de un 27 %. Los 18 participantes con audición bimodal mostraron mejor rendimiento con IC y audífono (Figura 2D, H) que con dos audífonos (Figura 2B, F). La mejora media fue de un 42 %.
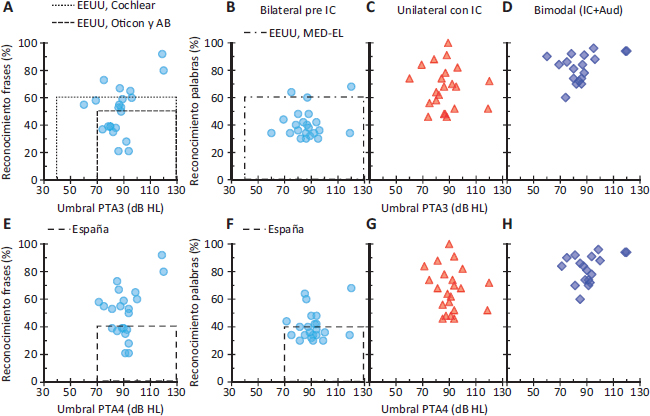
Figura 2. A. Reconocimiento de frases en silencio en la mejor condición de escucha (con dos audífonos) en función del PTA3 en el oído que posteriormente recibirá un IC (N=22). Los umbrales audiométricos se midieron sin amplificación. Las líneas de puntos y rayas representan los criterios actuales de indicación de IC según el país y la marca. Cinco participantes no cumplían con los criterios para recibir un IC de las marcas Cochlear, Oticon o Advanced Bionics en Estados Unidos. B. Como el panel A, pero para el reconocimiento de palabras CNC. C. Reconocimiento de palabras CNC en silencio tras recibir un IC (duración media de uso 17,9 meses). El reconocimiento se midió presentando las palabras sólo en el oído con IC, y se representa en función de los umbrales audiométricos obtenidos para el mismo oído antes de la implantación. D. Como el panel C, pero cuando los participantes usaban IC en un oído y audífono en el otro. E-H. Como los paneles A-D pero en función del PTA4. AB: Advanced Bionics. Datos obtenidos de Gifford et al. (2010).
En resumen, los resultados son consistentes con los de la Figura 1 e indican, por un lado, que personas con PTA3 ≥ 60 dB HL muestran mejor rendimiento con un IC y un audífono que con dos audífonos y, por otro, que incluso las personas que reconocen más de un 60 % de las frases pueden rendir mejor tras recibir un implante. Además, los resultados demuestran que el número de candidatos a IC sería mayor si se les evalúa con palabras en lugar de con frases, ya que el reconocimiento de palabras no está afectado por mecanismos compensatorios (como la inferencia de palabras por el contexto de la frase) que pueden ayudar a reconocer las frases de forma ‘ficticia’ (Gifford et al., 2008, 2010).
La FDA indica que la evaluación de un paciente que va a recibir un implante de MED-EL debe realizarse con palabras en lugar de frases. En concreto, el reconocimiento de palabras debe ser ≤ 50 % en el oído que se va a implantar y ≤ 60 % en el oído no implantado para que un adulto con pérdida auditiva bilateral reciba un implante de esta compañía (Tabla 1). Como referencia, hemos indicado el criterio de MED-EL como reconocimiento bilateral ≤ 60 % en la Figura 2B, ya que es probable que si el reconocimiento bilateral es ≤ 60 %, el reconocimiento en el oído no implantado o implantado también lo sea. Por tanto, todas las personas del estudio de Gifford et al. (2010), excepto dos, serían candidatas a IC de MED-EL en Estados Unidos. Desconocemos si esas dos personas cumplirían los criterios cuando se evalúa cada oído por separado.
En otro estudio, Amoodi et al. (2012) evaluaron a 27 adultos con edades de entre 26 y 89 años (media: 54,6 años) con pérdida auditiva bilateral moderada a profunda (PTA3 ≥ 55 dB HL). Dieciséis de ellos usaban audífonos en los dos oídos, 10 usaban audífono en un oído, y uno no usaba audífonos. Todos recibieron un IC (14 Advanced Bionics; 10 MED-EL; 3 Cochlear) entre los años 2000 y 2010, y 24 de ellos continuaron usando el audífono en el oído no implantado. Como puede observarse en la Figura 3A, ninguno de los participantes era candidato a IC en el momento del estudio porque mostraban un reconocimiento de las frases HINT mayor o igual al 60 % (círculos en Figura 3A). No obstante, todos mostraron mejor reconocimiento de frases tras recibir un IC (diamantes en Figura 3A). La mejora fue de un 27 % en promedio. Al igual que ocurría en el estudio de Gifford et al. (2010), los participantes mostraban peor rendimiento en el reconocimiento de palabras (círculos en Figura 3B) que en el de frases (círculos en Figura 3A), por lo que muchos de los participantes serían considerados candidatos a IC si se evaluaran de esta manera. Todos los participantes mostraron mejor reconocimiento de palabras tras recibir un IC sin llegar al 100 %, es decir, sin observarse un efecto techo (diamantes en Figura 3B). La mejora media fue de un 37 %.
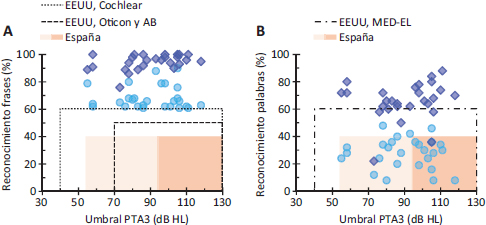
Figura 3. Reconocimiento de frases HINT (A) en silencio (N=19) o a una SNR de +5 dB (N=8) y reconocimiento de palabras CNC en silencio (B) en la mejor condición de escucha (dos oídos) antes (círculos) y 12 meses después (diamantes) de recibir un IC. El habla se presentó a 65 dB SPL. El reconocimiento se representa en función del umbral audiométrico PTA3 del oído implantado antes de recibir el IC. Los umbrales audiométricos se midieron sin amplificación. Las líneas de puntos y rayas indican los criterios de indicación de IC actuales, según el país y la marca. El área naranja oscuro indica que una persona con ese PTA3 recibiría un IC en España, y el área naranja claro, indica que es posible que una persona con ese PTA3 reciba un IC en España, dependiendo de si al incluir el umbral a 4 kHz el PTA4 es >70 dB HL. Los criterios de España se indican para frases y palabras, ya que no se especifica si “prueba vocal” se refiere a unas o a otras (Tabla 1). AB: Advanced Bionics. Datos obtenidos de Amoodi et al. (2012).
El estudio de Amoodi et al. (2012) es consistente con el de Gifford et al. (2010). Por un lado, demuestra que personas actualmente no consideradas candidatas a IC porque muestran un reconocimiento de frases mayor al 60 % podrían rendir mejor con IC que con audífonos. Por otro lado, demuestra que el reconocimiento de palabras es más sensible para detectar posibles candidatos a IC, ya que no da lugar a efectos techo.
Por último, Quatre et al. (2020) evaluaron a personas que no cumplían los criterios de la Haute Autorité de Santé de Francia para recibir un IC, es decir, que no tenían hipoacusia neurosensorial bilateral de severa a profunda con discriminación del habla en silencio <50 % utilizando listas de palabras de Fournier o equivalente a 60 dB SPL con audífonos optimizados. Para el reconocimiento de palabras monosilábicas presentadas en campo libre, la puntuación mediana en la mejor condición de escucha fue del 41 % antes de recibir el IC y del 74 % un año tras recibir el implante (N=105 adultos). El reconocimiento de palabras bisílabas en la mejor condición de escucha pasó del 60 % al 90 % tras la implantación (N=160 adultos).
Una pregunta que surge de los estudios revisados es ¿qué personas se beneficiarían de recibir un IC si sólo tuviéramos en cuenta su reconocimiento de palabras en la mejor condición de escucha? Si consideramos los dos estudios que proporcionan datos individuales (Gifford et al., 2010, y Amoodi et al., 2012) y promediamos los datos de reconocimiento de palabras monosilábicas en la mejor condición de escucha tras recibir un IC, obtenemos que los participantes reconocen un 72 % de palabras en promedio, con una desviación estándar de 15 %. Por tanto, es de esperar que una persona con un reconocimiento de palabras ≤57 % (la media menos una desviación estándar) probablemente muestre una mejora significativa tras recibir un IC. Esto es consistente con los criterios que proponen algunos estudios actuales (véase la sección de Discusión).
Los datos presentados en los párrafos anteriores hacen referencia a población adulta. Una pregunta que debemos abordar es si la población pediátrica (<18 años) que no cumple los criterios actuales para recibir un IC también podría rendir mejor con IC que con audífono. Para contestar a esa pregunta, revisamos los datos de Carlson et al. (2015). En este estudio se seleccionaron 51 pacientes menores de edad que habían recibido un IC (edad en el momento de implantación entre 7 meses y 17,6 años; media: 8,3 años), pero no cumplían con las directrices de la FDA para recibirlo. Las directrices en el momento del estudio eran similares a las actuales (Tabla 1), excepto que no estaba indicada la implantación en caso de hipoacusia unilateral o asimétrica. Carlson et al. (2015) incluyeron en su estudio niños que cumplían con uno o ambos de los siguientes criterios: (1) un PTA3 inferior a 70 dB HL en uno o ambos oídos si tenían entre 2 y 17 años, o un PTA3 inferior a 90 dB HL si eran menores de 2 años; o (2) una puntuación de reconocimiento de palabras y/o frases superior al 30 % con la mejor ayuda auditiva disponible. Los pacientes se distribuyeron en cuatro grupos. El Grupo A incluía a pacientes con PTA3 <70 dB HL (o <90 dB HL para niños menores de 2 años) en el oído que se iba a implantar (N = 8). El Grupo B comprendía a pacientes que tenían PTA3 <70 dB HL (o <90 dB HL para niños menores de 2 años) en el oído contralateral (N = 19). El Grupo C incluía a pacientes que obtuvieron una puntuación superior al 30% en el oído que se iba a implantar en pruebas de palabras/frases apropiadas para la edad (N = 24). Por último, el Grupo D incluía a pacientes que obtuvieron una puntuación superior al 30 % en la condición de mejor escucha antes de la implantación (N = 42). Ninguno de los cuatro grupos era mutuamente excluyente.
El rango de umbrales audiométricos en el oído implantado y el reconocimiento de habla (palabras y frases) en la mejor condición de escucha para toda la muestra se representan en la Figura 4A (línea roja). Las puntuaciones preoperatorias en la mejor condición de escucha oscilaron entre el 22 % y el 96 % (media = 58 %) (línea roja en la Figura 4A), y las puntuaciones de reconocimiento del habla en el oído implantado oscilaron entre el 0 % y el 70 % (media = 25 %). Diecisiete meses después de recibir un IC (44 Cochlear, 13 Advanced Bionics, 6 MED-EL), el reconocimiento del habla medio fue del 88 % con el oído implantado (Figura 4B) y del 90 % en la condición bimodal (IC + audífono) (Figura 4C). Eso supuso una mejora en el reconocimiento del 63 % y 31 %, respectivamente. Además, a nivel grupal, los niños demostraron más de 1 año de crecimiento lingüístico por año natural tras recibir el IC.
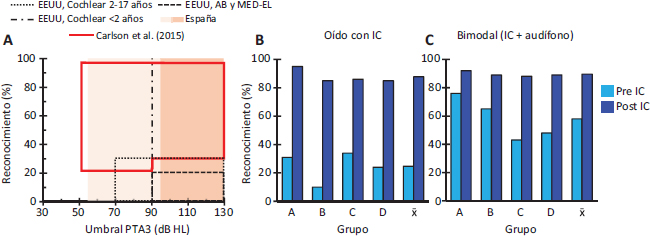
Figura 4. A. Características de los participantes incluidos en el estudio de Carlson et al. (2015) (línea roja). Las líneas de puntos y rayas indican los criterios actuales, según el país y la marca, para considerar a una persona con hipoacusia bilateral menor de 18 años como candidata a IC. El área naranja oscuro indica que una persona <18 años con ese PTA3 recibiría un IC en España, y el área naranja claro indica que una persona con ese PTA3 podría recibir un IC en España, dependiendo de si al promediar con 4 kHz el PTA4 es >70 dB HL. B. Rendimiento medio en las tareas de reconocimiento de palabras y frases antes (barras celestes) y después (barras azules) de recibir un IC. Resultados cuando los estímulos se presentaron en el oído implantado. Grupo A: PTA3 <70 dB HL (o <90 dB HL para niños menores de 2 años) en el oído con IC (N = 8). Grupo B: PTA3 <70 dB HL (o <90 dB HL en niños menores de 2 años) en el oído contralateral (N = 19). Grupo C: >30% de reconocimiento en el oído que se va a implantar en pruebas de palabras/frases apropiadas para la edad (N = 24). Grupo D: >30% en la mejor condición de escucha antes de la implantación (N = 42). x̄ = Media. C. Como el panel B, pero cuando el habla se percibía con dos oídos (IC y audífono contralateral). Datos obtenidos de Carlson et al. (2015). AB: Advanced Bionics.
El estudio de Carlson et al. (2015) demuestra que pacientes pediátricos que no cumplen los criterios actuales para recibir un IC muestran mejor reconocimiento con un IC que con amplificación, y los autores sugieren que “está justificada una reevaluación a gran escala de la candidatura pediátrica al IC, que incluya pérdidas auditivas menos graves y un mayor reconocimiento preoperatorio del habla para que más niños puedan beneficiarse de la implantación coclear”.
Los datos del estudio de Quatre et al. (2020), citado anteriormente, son consistentes con los de Carlson et al. (2015). Para la población pediátrica (edad <18 años), Quatre et al. (2020) indican que la puntuación mediana para el reconocimiento de palabras monosilábicas en la mejor condición de escucha aumentó del 48 % antes de la implantación al 82 % con el uso combinado de IC y audífono contralateral un año después de la implantación (N=35). En cuanto al reconocimiento de palabras bisílabas, el rendimiento aumentó del 80 % al 90 % tras la implantación (N=75).
Reconocimiento de habla en ruido
En los párrafos anteriores hemos analizado el beneficio que aporta el IC en el reconocimiento del habla en silencio en pacientes que no cumplen con los criterios para recibir este dispositivo. Sin embargo, es importante destacar que los usuarios de audífonos suelen experimentar mayores dificultades para reconocer el habla cuando ésta se presenta con ruido de fondo que cuando se presenta en silencio (Peters et al., 1998). Por ello, resulta relevante preguntarse si el IC también ofrece ventajas frente al audífono en condiciones ruidosas, especialmente en personas cuyo reconocimiento del habla en silencio es superior al umbral establecido por las guías clínicas actuales. Para responder esta pregunta, revisamos a continuación varios estudios que evaluaron el reconocimiento del habla tanto en silencio como en ruido en personas que no cumplían con los criterios de implantación vigentes en el país donde se llevaron a cabo las investigaciones.
Perkins et al. (2021) evaluaron a personas mayores de 16 años (edad promedio: 68 años) con pérdida auditiva postlocutiva que habían recibido uno (N=103) o dos (N=1) ICs entre 2009 y 2019. Los pacientes recibieron dispositivos de diferentes marcas: 42 recibieron Advanced Bionics, 34 Cochlear y 28 MED-EL. Para un subgrupo de pacientes, se evaluó tanto el reconocimiento de palabras CNC como de frases AzBio en silencio y a +5 dB SNR en ruido tipo “murmullo de hablantes” en la mejor condición de escucha. Las puntuaciones de reconocimiento del habla se obtuvieron antes de la implantación y a los 6 y/o 12 meses tras la activación del IC, según la disponibilidad de cada paciente. Todas las pruebas se realizaron con estímulos grabados a 60 dB SPL presentados a través de un único altavoz situado a 1 m de distancia frente al oyente. Además, se verificó que los audífonos proporcionaran la ganancia esperada según NAL-NL2 para el habla a 60 dB SPL.
La Figura 5A muestra que el reconocimiento de palabras en silencio mejoró del 52 % antes de la implantación al 75 % a los 6-12 meses tras la activación del IC (N=83). La Figura 5B muestra que la mayoría de los participantes mostró mejor reconocimiento tras recibir el IC (valores por encima de cero), y que la mejora aportada por el IC decrece cuanto mayor es el rendimiento antes de recibir el IC, no aportando beneficio a aquellas personas con un rendimiento pre-IC del 90 % (Figura 5A). Para las frases AzBio en silencio (N=80), la puntuación media aumentó del 70 % antes de la implantación al 87 % a los 6-12 meses tras la activación del IC (Figura 5C). Por otro lado, el beneficio aportado por el IC decrece al aumentar el rendimiento (Figura 5D), al igual que ocurre con las palabras. Además, la Figura 5C muestra que había más personas que mostraban un efecto techo (100 % de reconocimiento) antes de la implantación con frases que con palabras (Figura 5A), en consonancia con los estudios descritos en los apartados anteriores, y que pocas serían candidatas a IC si su rendimiento se evaluara con frases en silencio. No obstante, si su rendimiento se evaluara con frases en ruido, muchas de esas personas serían candidatas a IC (Figura 5E). Además, la mayoría de ellas obtendrían mejor rendimiento con un IC y un audífono que con dos audífonos (Figura 5F). Por lo tanto, los resultados sugieren que el IC puede mejorar significativamente el reconocimiento de habla en ruido.
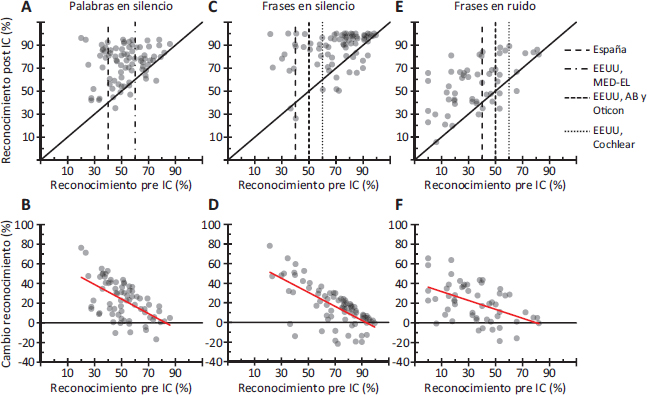
Figura 5. Paneles superiores: Reconocimiento de palabras CNC (A), frases AzBio en silencio (C), y frases AzBio en ruido +5 dB SNR (E) en la mejor condición de escucha antes y después de recibir un IC, es decir, con dos audífonos (pre-IC) frente a un IC y un audífono contralateral (post-IC). Las líneas verticales muestran los umbrales audiométricos que debe tener una persona adulta con pérdida auditiva bilateral para ser candidata a IC en diferentes países y para diferentes marcas (Tabla 1). AB: Advanced Bionics. Paneles inferiores: Cambio en el reconocimiento tras recibir un IC en función del reconocimiento que mostraba la persona antes de recibirlo. Los valores positivos representan mejor rendimiento con IC y audífono que con dos audífonos. Datos adaptados de Perkins et al. (2021).
El estudio de Mudery et al. (2016) muestra resultados consistentes con los de Perkins et al. (2021). Evaluaron a 15 pacientes (edad media: 73,3 años) que habían recibido un IC entre 2013 y 2015. Se evaluó el reconocimiento de frases AzBio de forma monoaural (solo audífono derecho o izquierdo) y bilateral. Si el paciente alcanzaba un rendimiento superior al 40 % en la mejor condición de escucha, se procedía a evaluar el reconocimiento de frases en ruido tipo “murmullo de hablantes” a +10 dB SNR. En caso de que el paciente superase el 40 % de reconocimiento en esta condición, se medía el reconocimiento de frases a una SNR de +5 dB. Las evaluaciones postoperatorias se realizaron a los 3, 6 y 12 meses tras la cirugía. Diez participantes fueron evaluados en silencio y en ruido, y todos, excepto uno, tenían un reconocimiento de frases preoperatorio con dos audífonos ≥58 % (media=74 %) en silencio. Tras recibir un IC, el reconocimiento de frases en la mejor condición de escucha aumentó un 10 % de media (desviación estándar 16 %) en silencio, y un 42 % (desviación estándar 33 %) en ruido. Al igual que en el estudio de Perkins et al. (2021), la mejora en el reconocimiento al recibir un IC decrecía al aumentar el rendimiento preoperatorio. Por tanto, los estudios de Mudery et al. (2016) y Perkins et al. (2021) demuestran que las personas con puntuaciones de reconocimiento de frases en silencio superiores al 60 % muestran mejor rendimiento con un IC y un audífono que con dos audífonos tanto para habla presentada en silencio como en ruido.
Satisfacción tras recibir un IC
A la hora de proporcionar el mejor tratamiento a un paciente, no sólo debe tenerse en cuenta la posible mejora en el reconocimiento del habla, sino también la posible mejora en la satisfacción con el dispositivo utilizado, así como en la calidad de vida. En este apartado analizamos la literatura para investigar si personas que no son candidatas a IC podrían estar más satisfechas y tener mejor calidad de vida utilizando un IC y un audífono que utilizando dos audífonos.
En el estudio de Amoodi et al. (2012), descrito anteriormente, se evaluó a un grupo de adultos con hipoacusia postlocutiva cuyo reconocimiento del habla superaba los criterios comúnmente aceptados para la implantación (Figura 2A), pero que estaban insatisfechos con sus audífonos. Se utilizó el cuestionario HHI (Hearing Handicap Inventory, Newman et al., 1991) para cuantificar el impacto emocional y social de la pérdida auditiva antes de la implantación y al año de recibir el IC. Encontraron que la puntuación en el cuestionario disminuyó significativamente tras recibir un IC (de 67,9 a 35,4 puntos), lo que indica una reducción significativa de la discapacidad auditiva autopercibida. Amoodi et al. (2012) argumentan que esa mejora se debe a que los participantes tenían problemas de reconocimiento del habla en su vida diaria con el uso de audífonos, algo que no se evidenció cuando se evaluó su rendimiento presentando frases del HINT en silencio.
Quatre et al. (2020) también evaluaron la calidad de vida de personas que no cumplían los criterios de la Haute Autorité de Santé de Francia para recibir un IC. Evaluaron a 270 pacientes adultos mediante la escala CAP (Categorical Auditory Performance; Archbold et al., 1995), una escala jerárquica que va de 1 a 7 y que evalúa el nivel de percepción auditiva funcional de una persona en situaciones de la vida diaria. La evaluación se realizó antes de la implantación coclear y un año después de esta. La puntuación mediana aumentó de 5 puntos antes de la implantación a 6 puntos tras la implantación. Esta diferencia fue estadísticamente significativa e indica que hubo una mejora en el nivel de percepción auditiva funcional tras recibir el IC. La media de las dificultades en la comunicación, evaluadas mediante el cuestionario APHAB (Abbreviated Profile of Hearing Aid Benefit; Cox y Alexander, 1995), fue del 53,4 % antes de la implantación y se redujo al 30,5 % tras un año de uso del IC. Los resultados también mejoraron en situaciones específicas. Concretamente, en entornos reverberantes las dificultades disminuyeron del 69,4 % al 56,3 %; en presencia de ruido de fondo pasaron del 73,4 % al 57,1 %; y en cuanto a la aversión a los sonidos, los valores bajaron del 46.7% al 41.4%. Para la población pediátrica (edad <18 años), Quatre et al. (2020) indican que 40 pacientes fueron evaluados con la escala CAP y que su puntuación mediana aumentó del 5 al 7 tras recibir un IC.
Aunque la evidencia es limitada, estos estudios muestran que los pacientes que se encuentran próximos a ser candidatos para recibir un IC podrían mostrar más satisfacción con ese dispositivo que con audífonos, especialmente cuando se encuentran insatisfechos con estos últimos.
Discusión
Criterios de indicación de IC propuestos
Los criterios de indicación del IC han ido cambiando a lo largo de los años. Actualmente no hay un criterio unificado a nivel internacional. Aunque la FDA indica que un adulto con pérdida auditiva bilateral es candidato para recibir un IC (de MED-EL o Cochlear) si tiene pérdida auditiva neurosensorial moderada (Tabla 1), en general, y en España en particular, se considera que una persona es candidata a IC cuando la pérdida auditiva es severa o profunda. En este artículo hemos analizado diferentes estudios que demuestran que personas con pérdida auditiva moderada podrían beneficiarse del uso de un IC. La Academia Americana de Otorrinolaringología y Cirugía de Cabeza y Cuello respalda que los niños mayores de 12 meses con umbrales audiométricos medios a cuatro frecuencias mayores a 65 dB HL y que muestren una “brecha persistente” o cada vez mayor en las habilidades auditivas y del lenguaje son aptos para la implantación (AAO-HNS, 2021). Los estudios de Leigh et al. (2016) (Figura 1A) y Zwolan et al. (2020) sugieren que los profesionales deberían considerar remitir a los pacientes para evaluar su candidatura a IC cuando tengan umbrales PTA3 > 60-65 dB HL. La literatura revisada en este estudio coincide con dichas recomendaciones (e.g., Amoodi et al., 2012; Gifford et al., 2010).
Otro de los criterios que debe cumplir una persona para ser candidata a IC es que su reconocimiento del habla en su mejor condición de escucha (en caso de pérdida auditiva bilateral) o en el oído a implantar (en caso de pérdida auditiva unilateral o asimétrica) sea menor a un determinado porcentaje que, de nuevo, varía de un país a otro (Tabla 1). Varios estudios han sugerido que la evaluación con las frases del HINT en silencio puede dar lugar a efectos techo y, en consecuencia, que esas frases no son apropiadas para realizar un seguimiento del rendimiento a lo largo del tiempo ni para determinar la candidatura para recibir un IC (Gifford et al., 2008; Firszt et al., 2004). Las frases AzBio son más difíciles de reconocer que las frases HINT, ya que ofrecen pistas contextuales limitadas, por lo que el paciente es menos capaz de predecir las palabras que no ha reconocido. Sin embargo, siguen teniendo suficiente contenido semántico para producir niveles más altos de reconocimiento en comparación con palabras monosilábicas (Gifford et al., 2008) (Figura 5). Algunos estudios sugieren adoptar el criterio de 60 % de reconocimiento en la mejor condición de escucha para considerar a una persona candidata a IC y que dicho criterio se evalúe con palabras monosilábicas (Zwolan et al., 2020; Zwolan y Basura, 2021) o presentando frases AzBio en ruido (Mudery et al., 2016; Zwolan y Basura, 2021). En línea con estas investigaciones, la batería “Minimum Speech Test Battery”, utilizada por los profesionales clínicos para la evaluación de la candidatura a IC en Estados Unidos, ha pasado de incluir las frases del HINT a las frases AzBio. Estas pruebas se añaden a la de reconocimiento de palabras monosilábicas, que se incluía en la batería desde un inicio (Zwolan y Basura, 2021; Dunn et al., 2024). En español tenemos grabadas las frases AzBio (Rivas et al., 2021) y palabras bisílabas (Cárdenas y Marrero, 1994; Weisleder y Hodgson, 1989), pero no hemos encontrado una prueba de palabras monosilábicas disponible (revisado por Rodríguez-Ferreiro y Serra, 2024). Velandia et al. (2024) compararon el reconocimiento de palabras monosilábicas CNC en inglés con el de palabras bisílabas en español (Weisleder y Hodgson, 1989) y encontraron que las palabras bisílabas daban lugar a un mayor porcentaje de reconocimiento. Sería conveniente, por lo tanto, desarrollar material en español para evaluar la candidatura a IC en personas de habla hispana de diferentes países.
Personas que reciben un IC en la actualidad
La evidencia aportada indica que los pacientes que no cumplen los criterios actuales para recibir un IC, pero que están próximos a cumplirlos, deberían derivarse para su evaluación como candidatos al implante, ya que probablemente obtendrán mayor beneficio de dicho implante que del audífono. Esta evidencia está en sintonía con las decisiones que toman los otorrinos estadounidenses a la hora de implantar a un paciente, ya que más de tres cuartas partes de los cirujanos entrevistados afirman realizar la implantación coclear al margen de los criterios oficiales de la FDA (Carlson et al., 2018). Por otro lado, esto contrasta con el hecho de que menos del 10 % de las personas con hipoacusia severa o profunda reciben un IC (2.1 % en Estados Unidos, 3 % en España, 5 % en Reino Unido, 5,7 % en Bélgica y Países Bajos) (Beraza-Tamayo et al., 2023). Estos datos demuestran que miles de personas en el mundo no están recibiendo el mejor tratamiento para su pérdida auditiva.
Limitaciones
El objetivo de este artículo es aportar una perspectiva basada en la evidencia sobre si las personas ‘límite’ que no llegan a cumplir los criterios actuales de implantación podrían rendir mejor con ICs que con audífonos. Nos hemos centrado en analizar la evidencia relativa a personas con pérdida auditiva bilateral a las que se les implantó un solo IC, ya que es el caso más común y también sobre el que existe más evidencia. La evidencia sobre otros casos es escasa o nula. Por ejemplo, en relación con las personas con pérdida auditiva unilateral o asimétrica, solo hemos encontrado un estudio relevante (Bernstein et al., 2025). Dicho estudio analizó personas con pérdida unilateral o asimétrica (PTA4 ≥ 59 dB HL y reconocimiento de palabras CNC >5 % y <40 % en el oído a implantar) que no cumplían los criterios actuales de implantación en Estados Unidos (Tabla 1). Se observaron mejoras notables al usar solo el IC, tanto en la comprensión del habla como en la capacidad para localizar sonidos, así como en la calidad de vida percibida. Estos beneficios fueron comparables a los de pacientes con pérdida auditiva unilateral o asimétrica que cumplieron el umbral de reconocimiento del 5 %. El estudio sugiere, por tanto, flexibilizar los criterios para determinar los candidatos a IC en casos de pérdida auditiva unilateral o asimétrica.
Respecto al uso de dos ICs en personas con pérdida auditiva bilateral que se consideran candidatos ‘límite’, no hemos encontrado estudios relevantes.
En cuanto a la población pediátrica, se han revisado tres estudios (Carlson et al., 2015, Leigh et al., 2016, Quatre et al., 2020). Queremos destacar especialmente el de Carlson et al. (2015) ya que hace referencia a los criterios en Estados Unidos, que se encuentran entre los más restrictivos. Carlson et al. (2015) demuestran que aquellos usuarios de audífonos con una puntuación de reconocimiento de habla superior al 30 % muestran mejor rendimiento con IC y audífono contralateral que con dos audífonos, además de mostrar un mayor desarrollo lingüístico. Este estudio señala como una paradoja el hecho de que las exigencias para la implantación coclear sean más estrictas en niños que en adultos (Tabla 1), cuando los primeros años de vida son fundamentales para el desarrollo del lenguaje. Es necesario un mayor número de estudios para definir los criterios pediátricos en base a la evidencia científica.
Por último, cabe destacar que, aunque el IC podría beneficiar a personas que no cumplen los actuales criterios de implantación, el IC implica una intervención quirúrgica bajo anestesia general, lo que conlleva riesgos, así como una mayor rehabilitación audiológica que el audífono. Esto se traduce en un mayor coste inicial del IC (Benifla et al., 2024), algo que debe considerarse especialmente en regiones con menores ingresos. No obstante, aunque hay que tener en cuenta las particularidades de cada país, en general, el IC es una intervención ventajosa en términos de coste-beneficio a largo plazo (Gatto et al., 2024; Neve et al., 2021).
Conclusiones
Hemos investigado si el rendimiento con un IC es mejor que con uno o dos audífonos en pacientes ‘límite’ que no llegan a alcanzar una hipoacusia severa. La evidencia científica analizada muestra que los pacientes con umbrales audiométricos PTA3 ≥ 65 dB HL tienen un 80 % de probabilidad de rendir mejor con un IC que con uno o dos audífonos. La evidencia también muestra que las personas con reconocimiento preoperatorio de palabras monosilábicas menor al 60 % en la mejor condición de escucha (con dos audífonos) mostrarán mayor rendimiento con IC y audífono contralateral que con dos audífonos. Por otro lado, la implantación en pacientes ‘límite’ reduce el impacto emocional y social de la pérdida auditiva y aumenta la calidad de vida de estas personas. Nuestra síntesis concuerda con estudios recientes e informes internacionales que sugieren que los profesionales deberían considerar remitir a los pacientes para evaluar su candidatura a IC cuando tengan umbrales audiométricos >60-65 dB HL y un reconocimiento de palabras <60 % en la mejor condición de escucha.
Referencias
Alkaf, F. M., y Firszt, J. B. (2007). Speech recognition in quiet and noise in borderline cochlear implant candidates. J Am Acad Audiol, 18(10), 872-82. https://doi.org/10.3766/jaaa.18.10.6
American Academy of Otolaryngology–Head and Neck Surgery (AAO-HNS) (2021). Position statement: Pediatric cochlear implantation candidacy. https://www.entnet.org/resource/position-statement-pediatric-cochlear-implantation-candidacy/
Amoodi, H. A., Mick, P. T., Shipp, D. B., Friesen, L. M., Nedzelski, J. M., Chen, J. M., y Lin, V. Y. (2012). Results with cochlear implantation in adults with speech recognition scores exceeding current criteria. Otol Neurotol, 33(1), 6-12. https://doi.org/10.1097/MAO.0b013e318239e5a1
Archbold, S., Lutman, M. E., y Marshall, D. H. (1995). Categories of Auditory Performance. Ann Otol Rhinol Laryngol 166, 312-314.
Benifla, M., Martelli, N., Brenet, E., Compagnon, C., Dubernard, X., y Labrousse, M. (2024). Costs analysis of cochlear implantation in children. European Annals of Otorhinolaryngology, Head and Neck Diseases, 141(4), 209-213. https://doi.org/10.1016/j.anorl.2024.02.012
Beraza-Tamayo, N., Cenjor-Español, C., Gómez-Pajuelo, P., Jáudenes-Casaubón, C., Manrique, M., Nuñez, F., de-Raeve, L., Ramos, A., y Zamora, J. (2023). Libro blanco sobre implantes cocleares en adultos y ancianos. GAES
Bernstein, J. G. W., Pillion, E. M., y Tolisano, A. M. (2025). Clinical Outcomes for Adult Single-Sided Deafness Cochlear. Implantees Exceeding the 5% Candidacy Criterion. Ear Hear, 46(2), 336-346. https://doi.org/10.1097/AUD.0000000000001578
British Deaf Association (2015). Fast facts about the Deaf community. https://bda.org.uk/fast-facts-about-the-deaf-community/
Byrne, D., Dillon, H., Ching, T., Katsch, R., y Keidser, G. (2001). NAL-NL1 procedure for fitting nonlinear hearing aids: characteristics and comparisons with other procedures. J Am Acad Audiol, 12(1), 37-51.
Cárdenas, M., y Marrero, V. (1994). Cuaderno de logoaudiometría. Universidad Nacional de Educación a Distancia.
Carlson, M. L., Sladen, D. P., Gurgel, R. K., Tombers, N. M., Lohse, C. M., y Driscoll, C. L. (2018). Survey of the American Neurotology Society on Cochlear Implantation: Part 1, Candidacy Assessment and Expanding Indications. Otol Neurotol, 39(1), e12-e19. https://doi.org/10.1097/MAO.0000000000001632
Carlson, M. L., Sladen, D. P., Haynes, D. S., Driscoll, C. L., DeJong, M. D., Erickson, H. C., Sunderhaus, L. W., Hedley-Williams, A., Rosenzweig, E. A., Davis, T. J., y Gifford, R. H. (2015). Evidence for the expansion of pediatric cochlear implant candidacy. Otol Neurotol, 36(1), 43-50. https://doi.org/10.1097/MAO.0000000000000607
Carlyon, R. P., y Goehring, T. (2021). Cochlear Implant Research and Development in the Twenty-first Century: A Critical Update. J Assoc Res Otolaryngol, 22(5), 481-508. https://doi.org/10.1007/s10162-021-00811-5
Cox, R. M., y Alexander, G. C. (1995). The abbreviated profile of hearing aid benefit. Ear Hear, 16(2), 176-86. https://doi.org/10.1097/00003446-199504000-00005
Davies-Venn, E., Souza, P., Brennan, M., y Stecker, G. C. (2009). Effects of audibility and multichannel wide dynamic range compression on consonant recognition for listeners with severe hearing loss. Ear Hear, 30(5), 494-504. https://doi.org/10.1097/AUD.0b013e3181aec5bc
Dorman, M. F., Loizou, P. C., Kemp, L. L., y Kirk, K. I. (2000). Word recognition by children listening to speech processed into a small number of channels: data from normal-hearing children and children with cochlear implants. Ear Hear, 21(6), 590-596. https://doi.org/10.1097/00003446-200012000-00006
Dunn, C. C., Zwolan, T. A., Balkany, T. J., Strader, H. L., Biever, A., Gifford, R. H., Hall, M. W., Holcomb, M. A., Hill, H., King, E. R., Larky, J., Presley, R., Reed, M., Shapiro, W. H., Sydlowski, S. A., Wolfe, J. (2024). A Consensus to Revise the Minimum Speech Test Battery-Version 3. Am J Audiol, 33(3), 624-647. https://doi.org/10.1044/2024_AJA-24-00008.
Firszt, J. B., Holden, L. K., Skinner, M. W., Tobey, E. A., Peterson, A., Gaggl, W., Runge-Samuelson, C. L., y Wackym, P. A. (2004). Recognition of speech presented at soft to loud levels by adult cochlear implant recipients of three cochlear implant systems. Ear Hear, 25(4), 375-87. doi: https://doi.org/10.1097/01.aud.0000134552.22205.ee
Food and Drug Administration (FDA). (2024). Summary of safety and effectiveness data: Premarket Approval Application (PMA) Number: P000025/S129. https://www.accessdata.fda.gov/scripts/cdrh/cfdocs/cfpma/pma.cfm?ID=P000025S129
Gatto, A., Tofanelli, M., Valentinuz, G., Mascherin, A., Costariol, L., Rizzo, S., Borsetto, D., Boscolo-Rizzo, P., y Tirelli, G. (2024). Cochlear implant cost analysis in adults: a European narrative review. Eur Arch Otorhinolaryngol, 281(9), 4455-4471. https://doi.org/10.1007/s00405-024-08591-3
Gifford, R. H., Dorman, M. F., Shallop, J. K., y Sydlowski, S. A. (2010). Evidence for the expansion of adult cochlear implant candidacy. Ear Hear, 31(2), 186-94. https://doi.org/10.1097/AUD.0b013e3181c6b831
Gifford, R. H., Shallop, J. K., y Peterson, A. M. (2008). Speech recognition materials and ceiling effects: considerations for cochlear implant programs. Audiol Neurootol, 13(3), 193-205. https://doi.org/10.1159/000113510
Hainarosie, M., Zainea, V., y Hainarosie, R. (2014). The evolution of cochlear implant technology and its clinical relevance. J Med Life, 7(Spec Iss 2), 1-4.
Johannesen, P. T., Pérez-González, P., y Lopez-Poveda, E. A. (2014). Across-frequency behavioral estimates of the contribution of inner and outer hair cell dysfunction to individualized audiometric loss. Front Neurosci., 8 214. https://doi.org/10.3389/fnins.2014.00214
Jorgensen, L. E., Benson, E. A., y McCreery, R. W. (2018). Conventional Amplification for Children and Adults with Severe-to-Profound Hearing Loss. Semin Hear, 39(4), 364-376. https://doi.org/10.1055/s-0038-1670699
Kirk, K. I., Pisoni, D. B., y Osberger, M. J. (1995). Lexical effects on spoken word recognition by pediatric cochlear implant users. Ear Hear, 16(5):470-81. https://doi.org/10.1097/00003446-199510000-00004
Leigh, J. R., Dettman, S. J., y Dowell, R. C. (2016). Evidence-based guidelines for recommending cochlear implantation for young children: Audiological criteria and optimizing age at implantation. Int J Audiol, 55(Suppl 2), S9-S18. https://doi.org/10.3109/14992027.2016.1157268
Leigh-Hunt, N., Bagguley, D., Bash, K., Turner, V., Turnbull, S., Valtorta, N., y Caan, W. (2017). An overview of systematic reviews on the public health consequences of social isolation and loneliness. Public Health 152, 157-171. https://doi.org/10.1016/j.puhe.2017.07.035
Livingston, G., Huntley, J., Liu, K. Y., Costafreda, S. G., Selbæk, G., Alladi, S., Ames, D., Banerjee, S., Burns, A., Brayne, C., Fox, N. C., Ferri, C. P., Gitlin, L. N., Howard, R., Kales, H. C., Kivimäki, M., Larson, E. B., Nakasujja, N., Rockwood, K., …, y Mukadam, N. (2024). Dementia prevention, intervention, and care: 2024 report of the Lancet standing Commission. The Lancet, 404(10452), 572–628. https://doi.org/10.1016/S0140-6736(24)01296-0
Lopez-Poveda, E. A., Eustaquio-Martín, A., Fumero, M. J., Gorospe, J. M., Polo López, R., Gutiérrez Revilla, M. A., Schatzer, R., Nopp, P., y Stohl, J. S. (2020). Speech-in-noise recognition with more realistic implementations of a binaural cochlear-implant sound coding strategy inspired by the medial olivocochlear reflex. Ear and Hearing, 41(6), 1492-1510. https://doi.org/10.1097/AUD.0000000000000880
Lopez-Poveda, E. A., Eustaquio-Martin, A., Stohl, J. S., Wolford, R. D., Schatzer, R., Gorospe, J. M., Santa Cruz Ruiz, S., Benito, F., y Wilson, B. S. (2017). Intelligibility in speech maskers with a binaural cochlear implant sound coding strategy inspired by the contralateral medial olivocochlear reflex. Hearing Research, 348, 134-137. https://doi.org/10.1016/j.heares.2017.02.003
Lopez-Poveda, E. A., Eustaquio-Martin, A., Stohl, J. S., Wolford, R. D., Schatzer, R., y Wilson, B. S. (2016). A binaural cochlear implant sound coding strategy inspired by the contralateral medial olivocochlear reflex. Ear and Hearing, 37(3), e138-e148. https://doi.org/10.1097/AUD.0000000000000273
Lopez-Poveda, E. A., Johannesen, P. T., Pérez-González, P., Blanco, J. L., Kalluri, S., y Edwards, B. (2017). Predictors of hearing aid outcomes. Trends Hear, 21, 1-28. https://doi.org/10.1177/2331216517730526.
Manrique, M., Ramos, Á., de Paula Vernetta, C., Gil-Carcedo, E., Lassaletta, L., Sanchez-Cuadrado, I., Espinosa, J. M., Batuecas, Á., Cenjor, C., Lavilla, M. J., Núñez, F., Cavalle, L., y Huarte, A. (2017). Guía clínica sobre implantes cocleares. Acta Otorrinolaringol Esp, 70(1), 47-54. https://doi.org/10.1016/j.otorri.2017.10.007.
Mudery, J. A., Francis, R., McCrary, H., y Jacob, A. (2016). Older Individuals Meeting Medicare Cochlear Implant Candidacy Criteria in Noise but Not in Quiet: Are These Patients Improved by Surgery? Otol Neurotol, 38(2), 187-191. https://doi.org/10.1097/MAO.0000000000001271
National Institute for Health and Care Excellence (NICE) (2019). Cochlear implants for children and adults with severe to profound deafness (TA566). www.nice.org.uk/guidance/ta566
Neve, O. M., Boerman, J. A., van den Hout, W. B., Briaire, J. J., van Benthem, P. P. G., y Frijns, J. H. M. (2021). Cost-benefit Analysis of Cochlear Implants: A Societal Perspective. Ear Hear, 42(5), 1338-1350. https://doi.org/10.1097/AUD.0000000000001021
Newman, C. W., Weinstein, B. E., Jacobson, G. P., y Hug, G. A. (1991). Test-retest reliability of the Hearing Handicap Inventory for Adults. Ear Hear, 12, 355–357. https://doi.org/10.1097/00003446-199110000-00009
Nilsson, M., Soli, S. D., y Sullivan, J. A. (1994). Development of the Hearing in Noise Test for the measurement of speech reception thresholds in quiet and in noise. J Acoust Soc Am, 95(2), 1085-99. https://doi.org/10.1121/1.408469
Organización mundial de la salud (OMS) (2021). World report on hearing. https://www.who.int/publications/i/item/9789240020481
Organización mundial de la salud (OMS) (2025). Sordera y pérdida de la audición. https://www.who.int/es/news-room/fact-sheets/detail/deafness-and-hearing-loss
Park, L. R., Gagnon, E. B., y Brown, K. D. (2021). The Limitations of FDA Criteria: Inconsistencies with Clinical Practice, Findings, and Adult Criteria as a Barrier to Pediatric Implantation. Semin Hear, 42(4), 373-380. https://doi.org/10.1055/s-0041-1739370
Perkins, E., Dietrich, M. S., Manzoor, N., O’Malley, M., Bennett, M., Rivas, A., Haynes, D., Labadie, R., y Gifford, R. (2021). Further Evidence for the Expansion of Adult Cochlear Implant Candidacy Criteria. Otol Neurotol, 42(6), 815-823. https://doi.org/10.1097/MAO.0000000000003068
Peters, R. W., Moore, B. C., y Baer, T. (1998). Speech reception thresholds in noise with and without spectral and temporal dips for hearing-impaired and normally hearing people. J Acoust Soc Am, 103(1), 577-587. https://doi.org/10.1121/1.421128
Peterson, G. E., y Lehiste, I. (1962). Revised CNC lists for auditory tests. J Speech Hear Disord, 27, 62-70. https://doi.org/10.1044/jshd.2701.62
Quatre, R., Fabre, C., Aubry, K., Bordure, P., Bozorg-Grayeli, A., Deguine, O., Eyermann, C., Franco-Vidal, V., Godey, B., Guevara. N., Karkas, A., Klopp, N., Labrousse, M., Lebreton, J. P., Lerosey, Y., Lescanne, E., Loundon, N., Marianowski, R., …, y Schmerber, S. (2020). The French Cochlear Implant Registry (EPIIC): Cochlear implant candidacy assessment of off-label indications. Eur Ann Otorhinolaryngol Head Neck Dis, 137(Suppl 1), S27-S35. https://doi.org/10.1016/j.anorl.2020.07.012
Rivas, A., Perkins, E., Rivas, A., Rincon, L. A., Litvak, L., Spahr, T., Dorman, M., Kessler, D., y Gifford, R. (2021). Development and Validation of the Spanish AzBio Sentence Corpus. Otol Neurotol, 42(1), 154-158. https://doi.org/10.1097/mao.0000000000002970
Rodríguez-Ferreiro, M., y Serra, V. (2024). Pruebas de habla en ruido: una revisión de las pruebas disponibles en español. Auditio, 8, e113. https://doi.org/10.51445/sja.auditio.vol8.2024.113
Shukla, A., Harper, M., Pedersen, E., Goman, A., Suen, J. J., Price, C., Applebaum, J., Hoyer, M., Lin, F. R., y Reed, N. S. (2020). Hearing loss, loneliness, and social isolation: a systematic review. Otolaryngol Head Neck Surg 162, 622-633. https://doi.org/10.1177/0194599820910377
Souza, P. E., Boike, K. T., Witherell, K., y Tremblay, K. (2007). Prediction of speech recognition from audibility in older listeners with hearing loss: effects of age, amplification, and background noise. J Am Acad Audiol, 18(1), 54-65. https://doi.org/10.3766/jaaa.18.1.5
Summers, V., Makashay, M. J., Theodoroff, S. M., y Leek, M. R. (2013). Suprathreshold auditory processing and speech perception in noise: hearing-impaired and normal-hearing listeners. J Am Acad Audiol 24(4), 274-92. https://doi.org/10.3766/jaaa.24.4.4
Velandia, S. L., Prentiss, S. M., Martinez, D. M., Sanchez, C. M., Laffitte-Lopez, D., y Snapp, H. A. (2024). Classification performance of Spanish and English word recognition testing to identify cochlear implant candidates. Int J Audiolec, 1-7. https://doi.org/10.1080/14992027.2024.2427854
Weisleder, P., y Hodgson, W. R. (1989). Evaluation of four Spanish word-recognition-ability lists. Ear Hear 10(6), 387-92. https://doi.org/10.1097/00003446-198912000-00012
Zhang, Y., Johannesen, P. T., Molaee-Ardekani, B., Wijetillake, A., Attili Chiea, R., Hasan, P.-Y., Segovia-Martínez, M., y Lopez-Poveda, E. A. (2025). Comparison of performance for cochlear-implant listeners using audio processing strategies based on short-time FFT or spectral feature extraction. Ear Hear 46(1), 163-183. https://doi.org/10.1097/AUD.0000000000001565
Zwolan, T. A., y Basura, G. (2021). Determining Cochlear Implant Candidacy in Adults: Limitations, Expansions, and Opportunities for Improvement. Semin Hear, 42(4), 331-341. https://doi.org/10.1055/s-0041-1739283
Zwolan, T. A., Schvartz-Leyzac, K. C., y Pleasant, T. (2020). Development of a 60/60 Guideline for Referring Adults for a Traditional Cochlear Implant Candidacy Evaluation. Otol Neurotol, 41(7), 895-900. https://doi.org/10.1097/MAO.0000000000002664
Conflicto de interés
Los autores declaran no tener ningún conflicto de interés.
Contribuciones de los autores
Los autores han contribuido por igual al trabajo.
Financiación
Esta investigación ha sido posible gracias a la Junta de Castilla y León y el Fondo Europeo de Desarrollo Regional (Unidad de Excelencia iBrains-IN-CyL, ref. CLU-2023-1-01). Los costes de edición y publicación han sido subvencionados por MED-EL GmbH. El contenido del artículo ha sido elaborado de forma independiente, sin la influencia de ninguna empresa de audífono o implante coclear.
Agradecimientos
Agradecemos a Milagros J. Fumero y Almudena Eustaquio-Martín sus comentarios y correcciones al texto.
Oficina Editorial
Corrección: Rita López
Producción: Glaux Publicaciones Académicas